- Home »
- HomeStöd & Hopp » ImmunterapiPage 5
Immunterapi
Det pratas mycket om immunterapi som är ett relativt nytt och för vissa cancerdiagnoser framgångsrikt sätt att behandla cancer. Här får ni veta lite mer om vad det är och hur det fungerar.
Stöd & Hopp
- Telefonstöd
- Ring PALEMA
- Diskutera på Facebook
- Dina rättigheter
- Träning – fysisk och mental
- Kost vid cancer
- Om att behöva vara projektledare
- För dig som anhörig
- Checklista för cancerdrabbade
- Immunterapi
- Nya studier och forskning
- Palliativ vård
- Mat- och toakort
- Ordlista och förkortningar
- Överlevare
- Regionala avdelningar
- Andra aktörer
Vad är immunterapi?
Immunterapi är ett sätt att få kroppens immunförsvar att angripa cancerceller. Att utnyttja kroppens immunförsvar mot cancerceller är ett område där utvecklingen gått framåt med stormsteg på senare år.
Immunförsvaret är kroppens skydd mot ämnen som framkallar sjukdom. Det består bland annat av olika vita blodkroppar, celler som är specialiserade på att känna igen främmande ämnen som virus och bakterier och oskadliggöra dem.
Tanken med immunterapi är att trimma immunförsvaret så att det blir bättre på att bekämpa tumörceller, som annars är experter på att undkomma försvaret.
Hur fungerar det?
Ett sätt att få fart på immunförsvaret mot cancer är att använda antikroppar. Dessa är uppbyggda av proteiner och är en del av immunförsvaret. De kan också tillverkas utanför kroppen och ges i form av läkemedel.
Antikroppar binder till specifika molekyler på ytan av en cancercell och fungerar som markörer för var immunförsvarets T-celler (en slags vita blodkroppar) ska gå till attack.
Det finns redan en rad cancerläkemedel som är baserade på antikroppar och ännu fler är på väg.
Så går immunterapi till
Ska du genomgå immunterapi? Här får du se hur olika varianter av behandlingen kan gå till:
Checkpointhämmare
De senaste åren har en ny typ av läkemedel tillkommit som kallas checkpointhämmare. Det är antikroppar som riktar in sig på speciella molekyler på T-cellerna. Dessa molekyler bromsar vanligtvis T-cellerna. Genom att blockera den här ”bromsen” med en antikropp blir cellerna mer aggressiva mot cancern.
Det finns olika typer av checkpointhämmare, som CTLA4-antikroppar, PD-1-antikroppar och PD-L1-antikroppar.
Den här typen av läkemedel ges som dropp och har redan haft stor betydelse för patienter med bland annat malignt melanom och lungcancer. De testas vid allt fler diagnoser.
Biverkningar
På grund av hur checkpointhämmarna fungerar kan de ge biverkningar genom att de stimulerar immunförsvaret. Biverkningarna är ofta lindriga, men kan bli allvarliga och behöva behandlas. De vanligaste biverkningarna du kan drabbas av är:
- Diarré och i vissa fall inflammation av tarmslemhinnan.
- Reaktioner i huden som eksem, rodnad, klåda, utslag och nässelfeber.
- Inflammation i lungsäcken som kan ge hosta och andfåddhet.
- Hepatit – inflammation i levern. Leverprover följs regelbundet.
Behandlingen kan skilja sig åt beroende på hur svåra biverkningar någon får. Biverkningarna kan behandlas med kortison och/eller att man gör uppehåll i immunterapibehandlingen.
CAR-T
En annan metod är CAR-T, där man förstärker immuncellerna utanför kroppen. Det här testas bland annat på patienter med hudcancer.
Vita blodkroppar, framförallt T-celler, tas från tumörvävnad eller från blodet och modifieras genetiskt så att de blir mer effektiva på att bekämpa cancerceller. De modifierade cellerna brukar kallas CAR-T-celler, där CAR är namnet på ett speciellt protein på cellernas yta som känner igen tumörceller. Cellerna odlas och blir fler innan de ges tillbaka till patienten.
Det finns ett antal läkemedel som bygger på den här mekanismen. Läkemedlen används till vissa former av blodcancer.
Innan du genomgår en CAR-T-behandling kommer du att få cytostatika under tre dagar. Den fjärde dagen får du dina CAR-T-celler via ett dropp.
Biverkningar
När T-cellerna dödar cancercellerna bildas många cytokiner. Det kan leda till en ”cytokinstorm”, så kallad CRS (Cytokine Releasing Syndrom). Ibland kan CRS upplevas som influensaliknande symtom, men hur allvarliga biverkningarna är kan variera från person till person. Cytokinstormen kan stoppas med blockerande läkemedel.
Efter att du har skrivits ut från sjukhuset måste du ändå hålla dig i sjukhusets närhet under ungefär fyra veckor. Det kan innebära att du måste bo på ett patienthotell, om ditt hem ligger långt bort från vården.
Vaccin mot cancer
Vaccin är också en form av immunterapi, som aktiverar immunförsvaret. Det fungerar enkelt uttryckt så att kroppen får en del av det ämne som orsakar en sjukdom – på så vis väcks immunförsvaret och skyddar oss mot smitta.
Cancer smittar inte, men vissa cancerformer kan orsakas av smittsamma virus, till exempel livmoderhalscancer. Därför vaccineras idag flickor och pojkar i skolåldern, vilket kommer att minska insjuknandet i den cancerformen.
Vaccination mot hepatit, som infekterar levern, skulle också kunna förebygga många fall av levercancer världen över. Men det finns också så kallade cancervacciner som ges som behandling när en cancer redan utvecklats.
Vaccinet kan innehålla en viss slags immunceller (dentritceller), proteiner eller DNA från tumörceller.
Virus kan stimulera försvaret mot cancer
Virus är en orsak till flera cancerformer, till exempel är infektion med HPV (Humant Papillomvirus) nära kopplat till livmoderhalscancer och hepatit B till levercancer. Men virus kan också användas som ett vapen mot cancer genom att på olika sätt stimulera immunförsvaret.
I Uppsala pågår till exempel en studie där vanliga förkylningsvirus specialdesignas att leta upp och infektera cancerceller. Där förökar sig virusen tills de spränger cancercellerna. Det leder också till att immunförsvaret aktiveras. I början av 2017 behandlades den första patienten i Uppsalastudien.
Mångårig forskning bakom
Forskning om kroppens eget försvar mot cancer har pågått och stöttats av Cancerfonden i årtionden. Redan på 1960-talet visade cancerforskarna Georg och Eva Klein vid Karolinska institutet att tumörceller kan utlösa specifika immunreaktioner.
Även benmärgstransplantationer, som länge använts för att behandla leukemier, är en slags immunterapi.
De senaste åren har stora framsteg gjorts när det gäller att utnyttja kunskapen om immunsystemet för att utveckla nya cancerbehandlingar.
2013 utsågs immunterapi mot cancer till årets genombrott av tidskriften Science och 2018 belönades två forskare, James P. Allison och Tasuku Honjo, med Nobelpriset för sina insatser inom immunterapi.
I dag har flera effektiva immunterapeutiska behandlingar nått patienterna, och fler utforskas i studier världen över.
Cancerfonden finansierar en rad svenska forskningsprojekt om olika former av immunterapi. Flera av forskarna jobbar med olika varianter av CAR-T-celler och kroppens så kallade naturliga mördarceller, NK-celler.

Ovanstående information kommer från Cancerfonden.
Informationen här under kommer från varierande källor och är granskad av Angelica Selander, vår medlem och en spetspatient med mycket kunskap i ämnet.
Fungerar tyvärr inte för alla
Detta är ju en mycket spännande utveckling och en lovande behandlingsmöjlighet. Men det fungerar tyvärr inte lika bra för alla cancerdiagnoser eller alla individer.
Man har upptäckt hur immunterapi aktiverar immunsystemet för att känna igen och förstöra cancerceller hos vissa patienter men inte hos andra. Det verkar som om immunsystemet bara kan känna igen cancerceller som har särskilda genetiska mutationer. Först då kan kroppens immunsystem känna igen och attackera cancern när patienten får immunterapi.
Vissa cancerdiagnoser, som exempelvis bukspottkörtelcancer, fungerar det mindre bra för.
Förhoppningen är att få fram en behandling som i framtiden ger ett kraftfullt immunsvar vid en rad olika cancersjukdomar. För trots allt hjälper dagens immunterapi bara 20 procent av patienterna.
Biomarkörer
Vilka är då de mest betydelsefulla biomarköerna som är korrelerad med positiv effekt av immunterapi för pankreascancer enligt de senaste forskningsrönen?
Enligt de senaste forskningsrönen är de mest betydelsefulla biomarkörerna som är korrelerade med positiv effekt av immunterapi för pankreascancer:
- PD-L1 expression: Högre uttryck av PD-L1 har visat sig vara en stark biomarkör för positiv effekt av immunterapi vid behandling av pankreascancer.
- Tumörinfiltrerande lymfocyter (TILs): Närvaron av CD8-positive TILs och andra typer av TILs i tumören kan förutsäga en bättre respons på immunterapi.
- Microsatellitinstabilitet (MSI): MSI är en biomarkör som indikerar att tumören har en hög mutationstakt, vilket kan förbättra immunsvar.
- Mismatch repair deficiency (dMMR): Denna biomarkör indikerar att genetisk reparationsmekanism inte fungerar ordentligt och kan relateras till MSI
Dessa biomarkörer kan användas för att förutsäga vilka patienter som kommer att dra nytta av immunterapi vid behandling av pankreascancer.
Fler biomarkörer?
Det finns flera andra biomarkörer som kan påverka patienters svar på immunterapi, inklusive:
- Tumor mutational burden (TMB): högre TMB kan indikera en högre grad av mutationer i tumören vilket kan göra den mer mottaglig för immunterapi.
- PD-1 expression: högre uttryck för PD-1-receptorer på tumörceller och immunceller kan indikera ökad tumörinfiltrerande lymfocytaktivitet och därmed en mer gynnsam respons på immunterapi.
- Tumörinfiltrerande lymfocyter (TILs): högre grad av TILs kan indikera en förbättrad respons på immunterapi.
- Beta-2-microglobulin (B2M): högre B2M-nivåer kan signalera en mer immuntillgänglig tumörmiljö, vilket kan indikera en mer gynnsam respons på immunterapi.
- Cytokinprofil: vissa cytokiner, som IFN-gamma och IL-12, kan indikera en mer gynnsam respons på immunterapi.
- Genexression profil: vissa genuttryckmönster kan indikera en mer gynnsam respons på immunterapi, till exempel genuttryck för immunsuppressiva markörer som IDO1, TDO och VEGF.
Det är viktigt att notera att biomarkörer vanligtvis inte används ensamma för att förutsäga en patients respons på immunterapi, utan snarare används i kombination med andra kliniska och patologiska faktorer för att utveckla en mer omfattande prognos.
Mer om immuncheckpointhämmare
Immuncheckpoint-hämmare fungerar genom att blockera proteiner som kallas checkpointprotein eller PD-1 / PD-L1. Dessa proteiner sitter på ytan av cancerceller och hjälper dem att undvika immunsystemet. När checkpointproteinerna blockeras kan det naturliga immunsystemet identifiera och attackera cancer cellerna.
Det finns dock flera skäl till varför inte alla patienter med cancer svarar på immuncheckpointhämmare. En stor faktor är att cancer kan utveckla olika mekanismer för att undvika immunsystemet, även om checkpointproteinerna blockeras. Till exempel kan cancerceller förstärka andra hämmande signaler eller mutationer som gör dem immunologiskt tysta.
Andra faktorer som kan påverka patientens svar på immuncheckpointhämmare inkluderar tumörens histologi, graden av tumörmutational belastning, graden av immuncelsinfiltration och patientens immunsvar.
Därför är det svårt att förutsäga vilka patienter som kommer att svara på immuncheckpointhämmare, och det är viktigt att fortsätta forska för att förstå de underliggande mekanismerna som påverkar behandlingseffekten.

Kan strålning förstärka effekten av immunterapi/ immuncheckpointhämmare?
Det finns ett antal studier som tyder på att strålning kan förstärka immunterapins effekt genom att öka inflammatoriskt svar i tumörområdet, öka antigenpresentation och öka infiltrationen av immunceller till tumören.
En studie genomförd 2018 av The Lancet Oncology såg på effekten av strålning före immuncheckpointhämmare (ICIs) hos patienter med icke-småcellig lungcancer (NSCLC). Resultaten visade en signifikant ökning av överlevnad hos patienter som erhöll både strålning och ICIs jämfört med de som bara fick en av behandlingarna.
En annan studie från 2019 i tidningen Cancer Immunology, Immunotherapy visade att strålning tillsammans med en viss typ av immunoterapikombination ökade antalet CD8 + T-celler i tumörerna hos patienter med melanom. Detta resulterade i en överlevnadsfördel jämfört med de som bara fick immunterapi.
Därför finns det en stark evidens som tyder på att strålning kan förstärka effekten av immunterapi eller immuncheckpointhämmare.
Läs mer
Vilka är de senaste studierna gällande pankreascancer och immunterapi eller andra målinriktade terapier?
Det finns ett antal pågående studier gällande pankreascancer och immunterapi eller andra målinriktade terapier. Några av de senaste studierna inkluderar:
- En studie publicerad i New England Journal of Medicine 2021 visade att kombinationen av två immunhämmande terapier – pembrolizumab och ipilimumab – förbättrade överlevnadstiden hos patienter med metastaserande pankreascancer.
- En annan studie publicerad i Nature 2021 visade att ett inhibitoriskt protein som kallas TGF-beta kan blockera immunförsvaret och bidra till tumörexpression hos pankreascancer. Forskarna föreslog att en ny terapimetod som blockerar TGF-beta eller dess receptor kan ha potential att behandla sjukdomen.
- En pågående klinisk studie undersöker effekten av en målinriktad terapi, rubraca (ruccaparib), som riktas mot mutationer i BRCA1 / 2-generna. Studien inkluderar patienter med metastaserande pankreascancer som tidigare behandlats med kemoterapi.
- En annan studie pågår för att testa effektiviteten av en annan målinriktad terapi, olaparib, som riktas mot mutationer i BRCA1 /2-generna. Studien inkluderar patienter med inoperabel pankreascancer och kommer att utvärdera om olaparib kan förbättra deras överlevnadstid.
- En pågående studie undersöker möjligheten att använda immunoterapi för att förbättra effekten av strålbehandling vid behandling av lokalt avancerad pankreascancer. Studien testar en kombination av strålbehandling och ett immunhämmande läkemedel vid namn durvalumab.
Sammanfattningsvis pågår det ständigt nya studier för att hitta effektiva behandlingar för pankreascancer, inklusive immunterapi och målinriktade terapier. Resultaten av dessa studier innebär att behandlingsalternativet för denna dödliga sjukdom kan vara på väg att förbättras, även om det fortfarande är en svår cancer att behandla.
Abskopal effekt
Vad är abskopal effekt? Mycket förenklat:
Tidigare före introducering av immunterapi (immunchecheckpointhämmare) så såg man inte mycket av denna effekt vid strålning. Effekten innebär i korthet att om man strålar på ett ställe mot en specifik metastas/tumör så gav det även effekt mot övriga metastaser som inte var exponerade för strålning.
Men i takt med att immunterapi introducerades i cancervården har denna abskopala effekt visat sig mer betydelsefull.
Det har visat sig att tumörer som tidigare var “kalla” för immunterapi börjar svara på behandlingen när man kompletterar med strålning oavsett precisionsstrålning eller fältstråling/lågdosstrålning även om man bara strålar på ett specifikt ställe.
Abskopal effekt är en biologisk reaktion som ibland uppstår när en tumör bestrålas, där strålningen även påverkar tumörer i andra delar av kroppen som inte bestrålas direkt. Effekten kan ske på grund av ett immunologiskt svar i kroppen och kan resultera i minskade tumörstorlekar i de icke-bestrålade områdena.
Läs mer
- Abscopal Effect – an overview (engelska)
- A Review of the Abscopal Effect in the Era of Immunotherapy (engelska)
Senaste nytt om Immunterapi:
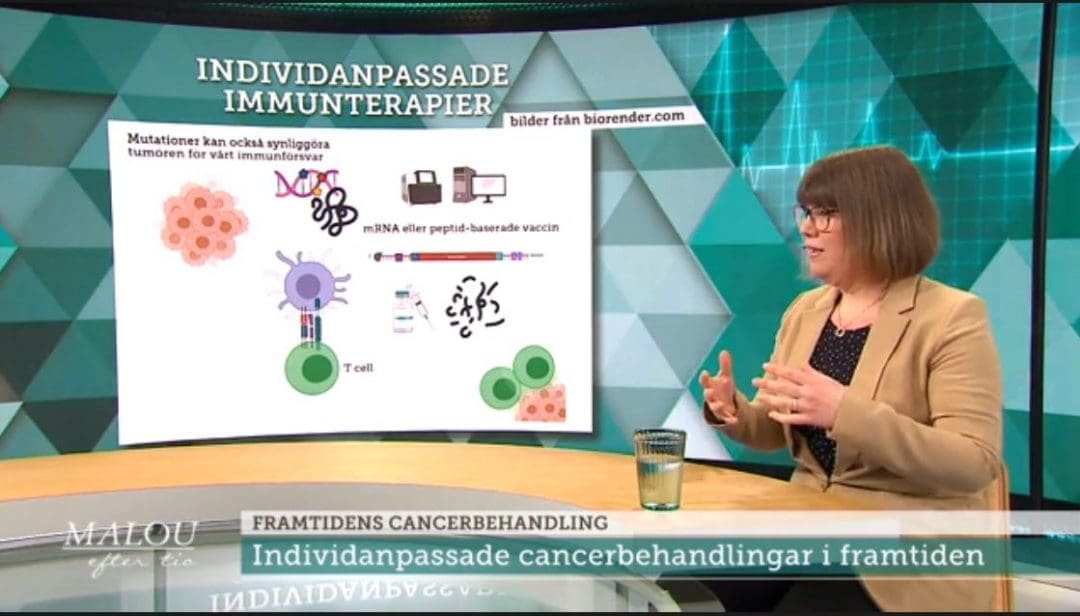
Individanpassad immunterapi kan bota cancer
2018 gick nobelpriset i medicin till immunterapi mot cancer. Sara Mangsbo som är en av de forskare som jobbar med flera olika typer av immunterapier pratar här hos Malou efter 10 i TV4 om individanpassade immunterapier.
15 september, 2021
Opdivo EU-godkänns mot återfall i matstrupscancer
Läkemedlet Opdivo har godkänts av EU-kommissionen som behandling mot återfall hos patienter med matstrupscancer eller cancer i övergången mellan matstrupe och magsäck.
10 augusti, 2021
Diskussioner om immunterapi och nya behandlingar – vad kan PALEMA göra?
Vi har under senaste tiden haft en intensiv diskussion på våra sociala media om immunterapi och nya behandlingar. Här kommer ett svar från PALEMA via vår ordförande Eva Backman.
21 december, 2020
Se inspelning från webbinarium – Det senaste inom kirurgi och immunterapi för pankreascancer
På Världspankreascancerdagen den 19 november höll vi månadens tredje webbinarium som handlade om det senaste inom kirurgi och immunterapi för pankreascancer. Nu kan ni se det i efterhand här.
30 november, 2020